中皮腫は、発生部位によって胸膜中皮腫、心膜中皮腫,腹膜中皮腫、及び精巣鞘膜中皮腫に分類されます。日本の死亡原因の第1位である悪性腫瘍による死亡者数は、2022年(令和4年)では 385,797人であり、そのうち中皮腫による死亡者数は1,554人(0.40%)でした。なお、現在では、中皮腫はそれらすべてが悪性として定義されているため、「Malignant:悪性」という用語は中皮腫を部位別に分類する際に使用されなくなり、米国の 2023NCCN (National Comprehensive Cancer Network Inc.)ガイドラインでもその記載方法に準拠しています。
中皮腫の80%以上は胸膜中皮腫ですが、腹膜中皮腫は中皮腫全体の約15%です。実際に、令和3年度に中皮腫として認定された患者さん679人の発症部位別の患者数は、胸膜610人、腹膜50人、その他(胸膜・腹膜,心膜,精巣鞘膜等)19人でした。腹膜中皮腫の男女比は3:2で胸膜中皮腫に比べて女性の割合が多く、胸膜中皮腫に比べて発症年齢が低いのが特徴です。米国の報告によると、腹膜中皮腫の診断時の平均年齢は約69歳で、患者の1年全生存率は約46%、5年全生存率は約20%です。
胸膜中皮腫の発症には石綿(アスベスト)曝露との因果関係が症例の80%以上で示されているのに対して、腹膜中皮腫では30~50%とされています。腹膜中皮腫の場合、胸膜中皮腫に比し高濃度の石綿曝露後に発生することが知られており、石綿曝露が腹膜中皮腫による死亡のリスクを上昇させることも知られています。曝露から発症までの潜伏期間は、胸膜中皮腫では平均約30~40年であるのに対して腹膜中皮腫では平均約20年と違いがあります。
このように、アスベスト曝露と中皮腫発症との関連性は胸膜と腹膜では異なるにもかかわらず、現在提唱されている病因仮説は同様とされています。発がん物質であるアスベストへの曝露により、DNA に損傷を与える小さな繊維粒子の沈着が惹起され、その結果酸素フリーラジカルが放出し、ゲノムの不安定性が生じると考えられています。そして、中皮細胞によって放出される活性酸素種と活性窒素種は、炎症反応を刺激し細胞増殖を促進することで、中皮細胞の発がんを刺激すると考えられます。
最近の分⼦生物学的研究により中皮腫に生じた遺伝⼦変異が明らかになりました。包括的なゲノム解析により、胸膜中皮腫では最も高頻度に不活性化する腫瘍抑制遺伝⼦として、 BAP1(約25-60%)、NF2(約40-50%)、CDKN2A(約70%以上)が明らかになりました。それらのうち、BAP1 と NF2 については、腹膜中皮腫においても⼀般的な遺伝⼦変異として同程度に認められますが、CDKN2A の欠損に関しては、その頻度は胸膜中⽪腫ほどに高くはないことが明らかとなっています。また、腹膜中皮腫では、胸膜中皮腫ではみられない ALK遺伝子の再構成が認められる症例が存在することや、患者さんの約50%はPD-L1発現が陽性で、他癌腫と同様にPD-L1の高発現症例も存在することが確認されています。
このように、腹膜中皮腫は、遺伝子変異の多様性によって特徴づけられ、びまん性、限局性、乳頭状などさまざまな組織型の間に分子的な違いが存在することも明らかにされています。
臨床症状は腹腔内の腫瘍量に関連し、患者は腹部腫瘤による腹痛,腹部膨満感、食欲不振、体重減少や腹水を訴えることが多いですが、発熱などで偶然発見される場合もあります。女性の腹膜中皮腫患者さんの場合ではしばしば婦人科を受診し婦人科腫瘍が疑われ、進行すると腫瘍が卵巣やその周辺臓器にも及びますが、それでも術前の画像診断では他の悪性腫瘍の腹膜播種との鑑別は難しく、そのまま婦人科腫瘍として手術されることがあります。
他の腹腔腫瘍と鑑別可能な特異的画像所見はなく,腹腔細胞診の診断精度も高くないため、診断の確定のためには組織診断が推奨されています。その生検部位の同定にはFDG-PETが有用であることが報告されています。
下段:症例提示:70歳男性 肉腫様腹膜中皮腫 (Dry‒painful type)
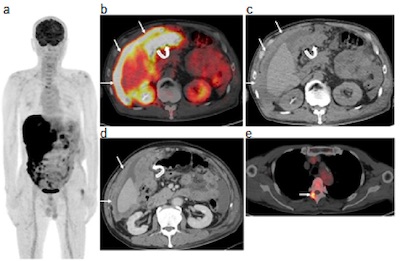
腹膜中皮腫は、臨床症状が非特異的で他の腹腔腫瘍と類似している一方で、その稀少性から診断確定はしばしば遅延します。症状が出てから確定診断までの平均期間は 4〜6か月とされますが、多くの場合さらに時間を要するのが実情です。
UICC(国際対がん連合)‒TNM 病期分類第8版において腹膜中皮腫のTNM分類は設定されていません。
腹膜中皮腫を対象として,PCI (Peritoneal carcinoma index) score による原発腫瘍の進展度(T),腹腔内リンパ節転移(N),腹腔外への腫瘍の広がり(M)を基にした新たな病期分類が提唱され,予後とよく相関するといわれていますが、本邦においてはその有用性は明らかではありません。
一方で、臨床病型分類として,CT 画像所見から腹水貯留を主とする wet type(腹水型),腫瘤形成を主とする dry‒painful type(腫瘤形成型),両者の特徴をもつ combined type(混合型)の3病型に分類する方法が用いられています。
肉眼所見としては、腫瘤が明らかでなく腹水のみのものから、腹膜の平坦病変、顆粒状変化、2 cm未満の単発ないし多発性腫瘤、びまん性腫瘤、腫瘤と腹腔内臓器が一塊化する例など症例により異なります。組織分類は胸膜中皮腫と同様ですが上皮様が圧倒的に多く、二相性の割合は胸膜中皮腫より少なく、純粋な肉腫様は極めて稀です。
また、腹膜封入嚢胞,アデノマトイド腫瘍,高分化乳頭状中皮腫瘍に類似した部分像を呈することや 異所性成分, 砂粒小体,リンパ球や組織球の著明な浸潤を伴うこともあります。稀な特殊型である脱落膜様の多くは石綿曝露の既往のない40歳以下の女性の腹膜に発生するとされています。
根治的治療法は存在せず、標準的治療法(外科治療,内科治療)も確立されていないのは世界共通ですが、その実状は諸外国と日本では大きく異なります。
切除可能と判断される腹膜中皮腫に対しては、適格基準【good PS:全身状態が良好, epithelioid:上皮様の組織型, unicavitary:単房性病変, etc.】を満たせば、国際腹膜播種腫瘍機構(PSOGI:the Peritoneal Surface Oncology Group International)は、腫瘍減量手術(CRS:CytoReductive Surgery)と腹腔内温熱化学療法(HIPEC:Hyperthermic IntraPeritoneal Chemotherapy)を標準治療として強く推奨し、2023NCCNガイドラインもそれに準拠しています。ただし、CRS/HIPECは、重篤な合併症や死亡に至る可能性もあり、技術の習得には少なくとも100例の症例が必要であるとの報告もあります。そのような背景から、本邦においてはCRSが施行可能な施設がほとんどなく、HIPECに保険適応がないことや疾患の治療法に対する知見も乏しいことから、根治的な手術的加療はほとんど把握されていないのが現状です。
内科治療としては、現時点で日本では,切除不能な胸膜中皮腫の1次治療として、イピリムマブ/ニボルマブ併用療法及びペメトレキセドとシスプラチンの併用療法(PC療法)、また、2次治療以降として、ニボルマブ単剤療法が承認されています。一方,胸膜中皮腫以外の非胸膜中皮腫(腹膜中皮腫、心膜中皮腫及び精巣鞘膜中皮腫)に対しては効能・効果として承認されている薬剤はこれまでは存在せず標準的治療法も確立されていませんでした。しかし,すべての中皮腫は,中皮細胞が無限の増殖能を獲得し悪性化しているという点で,発生部位の如何にかかわらず生物学的に同等であることから,非胸膜中皮腫に対しても、胸膜中皮腫と同様の治療が有効であることは以前より期待され、実際に,腹膜中皮腫を対象とした米国のNCCN ガイドラインversion 2. 2023 において、兵庫医科大学や国立がん研究センター中央病院など、日本で行われた腹膜中皮腫に対するPC療法の結果を引用して、「胸膜中皮腫に対する化学療法は、腹膜中皮腫,心膜中皮腫及び精巣鞘膜中皮腫にも使用できる」と記載されています。加えて、NCCN ガイドライン version 2. 2023では、腹膜中皮腫の治療薬として胸膜中皮腫を対象とした臨床試験成績を根拠にニボルマブ及びイピリムマブの併用療法が推奨され、実際に投与することが可能ですが、日本では非胸膜中皮腫に対するニボルマブ及びイピリムマブの併用療法は認められていません。
一方、腹膜中皮腫などの非胸膜中皮腫については、日本を含めた各国において、実臨床では胸膜中皮腫に準じて加療されてきた経緯や、非胸膜中皮腫が胸膜中皮腫と病理形態学的及び細胞生物学的に類似していること、及び腹膜中皮腫でもPD-L1発現が認められていることなどから、ニボルマブは非胸膜中皮腫においても有効性が期待できると考えられていました。実際に、化学療法歴の有無を問わない非胸膜中皮腫患者を対象としてニボルマブの有効性及び安全性を検討する医師主導国内第Ⅱ相試験(VIOLA試験)が実施されました。その結果、適格基準を満たす患者さん20例を対象として、測定可能病変を有する患者さんにおける奏効率は35.7%(5/14例)、薬物治療歴の有無別の奏効率については、薬物治療歴無で42.9%(3/7例)、薬物治療歴有で28.6%(2/7例)で薬物治療歴の有無を問わず奏効が確認されました。
VIOLA試験におけるニボルマブの安全性プロファイルは、これまでに報告されているニボルマブの臨床試験で認められていたものと同様で、この結果に基づきニボルマブは2023(令和5)年11月に腹膜中皮腫を含む非胸膜中皮腫に対して国内外で初の承認を取得し、これまで標準治療が確立されていなかった非胸膜中皮腫の新たな治療選択肢の一つになりました。同時に厚生労働省より公表されたニボルマブの最適使用推進ガイドラインの一つに悪性中皮腫(悪性胸膜中皮腫を除く)が加えられ、VIOLA試験の詳細がHCM-002 試験として記載されています。
近年の研究で、他の遺伝子変異を有しない若年の腹膜中皮腫の患者さん(40歳以下)25名のうち、2名(8%)でALK遺伝子の再構成が確認され、腹膜中皮腫において胸膜中皮腫では認められなかった発癌のドライバー遺伝子と考えられるSTRN-ALK 融合遺伝子が確認されました。
ALK遺伝子は、未分化大細胞リンパ腫ではNPM1、炎症性筋線維芽細胞腫瘍ではTPM3またはTPM4、非小細胞肺癌ではEML4、腎髄質癌ではVCLと融合することにより、ALK 融合遺伝子として発癌性を示します。必須癌増殖因子として異常なALK遺伝子を有する腫瘍を総称して「ALKoma(アルコーマ)」 と呼ぶことが以前より提案され、STRN-ALK 融合遺伝子を有する腹膜中皮腫も「ALKoma」に該当します。
EML4-ALK融合遺伝子を有する非小細胞肺癌にはALK-TKI(チロシンキナーゼ阻害薬)が高い治療効果を示すことが確認され、クリゾチニブ、アレクチニブなど既に5種類の阻害薬が承認されていて、それらの阻害薬は、「ALKoma」である腹膜中皮腫においても奏功する可能性が期待されています。
このように、治療選択肢を検討する目的から、腹膜中皮腫のような希少癌においては、がん遺伝子パネル検査を行う時期を常に念頭におく必要があると考えられます。
2024年1月19日
兵庫医科大学 中皮腫センター 栗林 康造